فرآیند تولید آمونیاک به روش هابر
فرآیند تولید آمونیاک به روش هابر یکی از روشهای مهم و صنعتی برای تولید آمونیاک (NH3) از نیتروژن (N2) گرفته شده از هوا و هیدروژن (H2) به عنوان ماده اولیه، است. این فرآیند به نام دانشمند آلمانی “فریتز هابر” نامگذاری شده است و یک نقطه عطف مهم در صنعت شیمی است.قابل ذکر است که این فرایند بهطور مشترک توسط دو شیمیدان آلمانی به نامهای فریتس هابر و کارل بوش که هر دو از برندگان جایزه نوبل شیمی بودند، ابداع شد.
در این فرآیند، از یک کاتالیزور فلزی از گروه فلزهای انتقال (معمولاً آهن) استفاده میشود تا واکنش هیدروژن با نیتروژن در دمای بالا و فشار بالا را تسهیل کند. این واکنش به صورت زیر انجام میشود:
N2 + 3H2 → 2NH3
در این واکنش، یک مولکول نیتروژن با سه مولکول هیدروژن واکنش میکند تا دو مولکول آمونیاک تولید شود. این واکنش انجام میشود تا دمای حدود ۴۵۰-۵۰۰ درجه سانتیگراد و فشار حدود ۲۰۰-۳۰۰ اتمسفر.
عواملی همچون دما، فشار، ترکیب آغازین هیدروژن و نیتروژن، و نوع کاتالیزور میتوانند بر کارایی و عملکرد این فرآیند تأثیر بگذارند. این فرآیند در صنایع کشاورزی (به عنوان منبع اصلی نیتروژن برای کودها)، صنایع پتروشیمی، تولید پلاستیکها، فرآوری فلزات و غیره استفاده میشود.
مراحل اصلی فرآیند هابر :
1. تولید گازهای تغذیه:
در ابتدا، گازهای تغذیه مورد نیاز برای واکنش تولید میشوند. نیتروژن گاز (N2) از هوا جداسازی میشود و هیدروژن گاز (H2) از منابع مانند گاز طبیعی، نفت، یا ذغال سنگ به دست میآید.
2. خالص سازی گازهای تغذیه:
گازهای تغذیه باید از آلایندهها و ناخالصیها پاکسازی شوند تا واکنش به خوبی انجام شود. این مرحله شامل حذف متان (CH4)، آب، دی اکسید کربن (CO2) و سایر آلایندهها است.
3. واکنش سنتز:
گازهای نیتروژن و هیدروژن در شرایط با فشار بالا و دمای بین 400-450 درجه سانتیگراد بر روی یک کاتالیزور فلزی (به عنوان مثال، اکسید آهن با مساعدت کبالت و پتاسیم) با هم واکنش میدهند. این واکنش شیمیایی مستقیم بین نیتروژن و هیدروژن برای تشکیل آمونیاک است:
N2 + 3H2 -> 2NH3
4. خنککردن و تجمع:
آمونیاک تولید شده به صورت گازی است و باید خنک شود تا به صورت مایع تجمع کند. این فرآیند از طریق گذراندن گازهای خروجی از یک سری سردکنندهها و تجمع در تانکهای خنک میتواند انجام شود.
5. جداسازی آمونیاک:
آمونیاک مایع از مواد جامد یا گازهای دیگر جدا میشود. این میتواند به وسیله تقطیر فراوری شود تا آمونیاک خالص به دست آید.
فرآیند هابر از تکنولوژی مهمی در صنعت شیمی است که نقش حیاتی در تولید آمونیاک و محصولات مشتق شده آن دارد. این فرآیند برای تولید کمکهای کشاورزی و مواد شیمیایی صنعتی بسیار اساسی است و بهبودهای مختلفی در زمینه بهرهوری و پایداری در طول سالها بهدست آمده است.
چالش اول :فراهم کردن شرایط مناسب برای انجام واکنش
برای انجام بهتر واکنش هابر و تولید آمونیاک در شرایط مناسب، مهمترین عوامل زیر را باید در نظر گرفت:
1. فشار: واکنش تشکیل آمونیاک در فشار بالا انجام میشود. معمولاً فشار بین 150 تا 300 بار استفاده میشود. فشار بالا بهبود راندمان و سرعت واکنش را تحت تأثیر قرار میدهد. افزایش فشار، تعادل واکنش را به سمت تشکیل آمونیاک منتقل میکند.
2. دما: دمای مناسب برای واکنش هابر بین 400-450 درجه سانتیگراد است. افزایش دما، سرعت واکنش را افزایش میدهد اما باعث کاهش بهرهوری میشود. بنابراین، یک تعادل باید بین دما و سرعت واکنش حفظ شود.
3. کاتالیزور: استفاده از کاتالیزورهای فلزی مانند اکسید آهن با مساعدت کبالت و پتاسیم در واکنش هابر بسیار مهم است. این کاتالیزورها سرعت واکنش را افزایش میدهند و در حفظ تعادل واکنش نیز نقش دارند.
4. نسبت مولار نیتروژن به هیدروژن: به منظور حصول بهرهوری بالا در تولید آمونیاک، نسبت مولار نیتروژن به هیدروژن باید بهدرستی تنظیم شود. نسبت مولار 1:3 (نیتروژن به هیدروژن) به طور معمول استفاده میشود.
5. حذف آلایندهها: گازهای تغذیه باید از آلایندهها مانند متان، آب و دی اکسید کربن پاکسازی شوند. حضور این آلایندهها ممکن است عملکرد کاتالیزور را تحت تأثیر قرار داده و بهرهوری را کاهش دهد.
استفاده از این شرایط مناسب به همراه کنترل دقیق فشار، دما و نسبت مولار میتواند به تولید آمونیاک با بهرهوری بالا و کیفیت مناسب منجر شود.
چالش دوم : جداسازی آمونیاک
جداسازی آمونیاک پس از تولید آن در فرآیند هابر، به منظور به دست آوردن آمونیاک خالص استفاده میشود. برای جداسازی آمونیاک، میتوان از روشهای زیر استفاده کرد:
1. تقطیر: این روش شامل استفاده از تغییر دما و فشار است تا آمونیاک به صورت مایع جدا شود. در این روش، گاز آمونیاک با کاهش دما و افزایش فشار به شرایط مایع تبدیل میشود و سپس میتوان آن را جدا کرد.
2. جذب: در این روش، یک حلال خاص به نام حلال جذبکننده (مثل آب) برای جذب آمونیاک استفاده میشود. گاز آمونیاک از محیط عبور میکند و در تماس با حلال جذبکننده قرار میگیرد. سپس با تغییر شرایط، میتوان آمونیاک را از حلال جدا کرد.
3. انتقال غشا: در این روش، از غشاهای نیمه نفوذپذیر برای جداسازی آمونیاک استفاده میشود. گاز آمونیاک از یک طرف غشا عبور میکند در حالی که مولکولها و یونهای آمونیاک در غشا تحت تأثیر انتقال مییابند. به این ترتیب، میتوان آمونیاک را از سایر مواد جدا کرد.
4. کریستالیزاسیون: این روش شامل تشکیل بلورهای آمونیوم کلراید (NH4Cl) از گاز آمونیاک است. بلورهای تشکیل شده سپس جدا شده و تحت شرایط دیگری به آمونیاک خالص تبدیل میشوند.
ترکیبی از این روشها ممکن است در فرآیند جداسازی آمونیاک به کار رود. استفاده از روش مناسب و بهینه بستگی به شرایط صنعتی، اقتصادی و میزان خلوص مورد نیاز برای آمونیاک دارد.
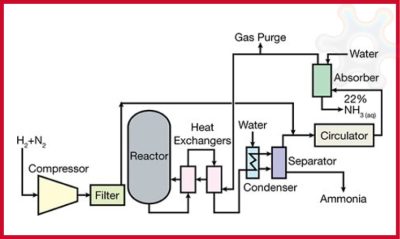
هابر
عناصر موجود در فرآیند هابر:
در فرآیند هابر برای تولید آمونیاک، عناصر زیر نقش مهمی ایفا میکنند:
1. نیتروژن (N2): نیتروژن یکی از مواد تغذیه اصلی در واکنش هابر است. این گاز از هوا استخراج میشود و به عنوان یکی از مواد اولیه اصلی در تولید آمونیاک استفاده میشود.
2. هیدروژن (H2): هیدروژن نیز به عنوان ماده تغذیه اصلی دیگر در فرآیند هابر مورد استفاده قرار میگیرد. این گاز از منابع مانند گاز طبیعی، نفت یا ذغال سنگ تولید میشود و با نیتروژن برای تشکیل آمونیاک واکنش میدهد.
3. کاتالیزورها: کاتالیزورها نقش مهمی در فرآیند هابر دارند. معمولاً اکسید آهن با مساعدت کبالت و پتاسیم به عنوان کاتالیزورها در این فرآیند استفاده میشوند. آنها کمک میکنند تا سرعت واکنش افزایش یابد و در حفظ تعادل واکنش نیز نقش دارند.
4. آلایندهها: در فرآیند هابر، حضور آلایندهها مانند متان، آب و دی اکسید کربن ممکن است عملکرد کاتالیزور را تحت تأثیر قرار داده و بهرهوری را کاهش دهد. بنابراین، حذف این آلایندهها از مواد تغذیه بسیار مهم است. مجموعهای از این عناصر در فرآیند هابر بهکار گرفته میشوند تا تولید آمونیاک با بهرهوری بالا و کیفیت مناسب انجام شود.
نسبت ترکیبات عناصر در واکنش
در واکنش هابر برای تولید آمونیاک، نسبت ترکیبات عناصر به صورت مفصل به دو صورت اعلام میشود: نسبت مولار و نسبت وزنی.
1. نسبت مولار: در این حالت، نسبت تعداد مولکولهای مواد در واکنش را مشخص میکنیم. به طور کلی، نسبت مولار ترکیبات عناصر در واکنش هابر به صورت 1:3 است. بنابراین، برای هر مولکول نیتروژن (N2)، سه مولکول هیدروژن (H2) به عنوان مواد اولیه مورد استفاده قرار میگیرند. این نسبت مولار به دلیل تعادل شیمیایی و بهرهوری بهینه در تولید آمونیاک تعیین شده است.
2. نسبت وزنی: در این حالت، نسبت جرم یا وزن مواد مورد استفاده در واکنش را مشخص میکنیم. برای نسبت وزنی ترکیبات عناصر در واکنش هابر، نسبت وزنی نیتروژن به هیدروژن برابر با 14:3 است. بنابراین، برای هر 14 واحد وزنی نیتروژن، 3 واحد وزنی هیدروژن به عنوان مواد اولیه استفاده میشوند.
به طور خلاصه، نسبت ترکیبات عناصر در واکنش هابر به صورت مفصل به دو صورت نسبت مولار 1:3 و نسبت وزنی 14:3 تعیین میشود. این نسبتها برای حفظ تعادل واکنش، بهرهوری بهینه و کنترل کیفیت محصول بسیار مهم هستند.
کاربرد تولید آمونیاک به روش هابر در صنایع:
روش هابر برای تولید آمونیاک دارای کاربردهای متعددی در صنعت و زندگی روزمره است. برخی از اصلیترین کاربردهای این روش عبارتند از:
1- تولید کودها: آمونیاک به عنوان منبع نیتروژن برای تولید کودها و محصولات کشاورزی مورد استفاده قرار میگیرد. کودهای حاوی آمونیاک به گیاهان نیتروژن لازم برای رشد و توسعه را میرسانند.
2- صنعت پتروشیمی: آمونیاک یک ماده اولیه مهم برای تولید محصولات پتروشیمی مانند اوره، مواد شیمیایی آلی و پلاستیکها است.
3- تولید اوره: آمونیاک به عنوان ماده اولیه برای تولید اوره (NH2CONH2) استفاده میشود، که در تولید کودهای نیتروژنه و محصولات شیمیایی دیگر کاربرد دارد.
4- صنعت فولاد: آمونیاک به عنوان منبع نیتروژن برای فرآیند کربوریزه کردن فولاد (تصفیه فلز آهن) مورد استفاده قرار میگیرد.
5- تولید اسید نیتریک: اسید نیتریک (HNO3) از آمونیاک به وسیله واکنش با اکسیژن تولید میشود. اسید نیتریک در صنایع شیمیایی و تولید کودها استفاده میشود.
6- تولید انرژی: آمونیاک همچنین به عنوان حامل نیتروژن در سیستمهای ذخیره انرژی، مانند سیستمهای انرژی هیدروژنی، مورد استفاده قرار میگیرد.
7-تولید مواد شیمیایی آلی: آمونیاک به عنوان ماده اولیه برای تولید مواد شیمیایی آلی مانند ملامین، مورفولین و امیدها استفاده میشود.
8-تصفیه آب: آمونیاک در فرآیندهای تصفیه آب به عنوان یک ماده مختزلکننده استفاده میشود تا مواد آلی و مواد مختلف زاید از آب حذف شوند.
این کاربردها تنها بخشی از کاربردهای فرآیند تولید آمونیاک به روش هابر هستند و اهمیت این فرآیند در صنایع مختلف به دلیل تأمین نیتروژن و آمونیاک به محصولات مختلف بسیار بزرگ است.
کاربرد تولید آمونیاک به روش هابر در صنعت خودرو سازی:
در صنعت خودروسازی، در بخشهایی از تولید خودرو و فرآیندهای مرتبط با آن، مصرف محصولات مشتق شده از آمونیاک وجود دارد. برخی از موارد ممکن عبارتند از:
تصفیه گازهای خروجی: در فرآیندهای تولید خودرو، مخصوصاً در موتورهای دیزل، انتشار اکسیدهای نیتروژن (NOx) به عنوان آلایندههای محیطی ایجاد میشود. تجهیزات تصفیه اکسیدهای نیتروژن میتوانند از آمونیاک به عنوان عامل اختزال (SCR: انتخابی کاتالیتیک اختزال) برای کاهش این آلایندهها استفاده کنند. در این فرآیند، آمونیاک به عنوان ماده اختزالی با اکسیدهای نیتروژن واکنش میکند و نیتروژن مولکولر و آب تولید میشوند.
تولید محصولات پلاستیکی و لاستیکی: موادی که از آمونیاک و مشتقات آن تولید میشوند، میتوانند در تولید برخی از محصولات پلاستیکی و لاستیکی مورد استفاده قرار گیرند که در تجهیزات داخلی و خارجی خودروها استفاده میشوند.
تولید مواد شیمیایی مورد نیاز: برخی از مواد شیمیایی آلی که در تولید خودروها مورد نیاز هستند، از آمونیاک و مشتقات آن تولید میشوند. این مواد ممکن است در فرآیندهای رنگآمیزی، پوششدهی، پلاستیکسازی و غیره مورد استفاده قرار گیرند.
تصفیه گازهای خروجی به چه شکل است؟
تصفیه گازهای خروجی (Exhaust Gas Treatment) به منظور کاهش آلودگی هوا و کاهش انتشار آلایندههای محیطی مانند اکسیدهای نیتروژن (NOx) و ذرات معلق (جزء از مواد معلق در هوا) از خروجی موتورهای داخلسوزی، به کار میرود. یکی از روشهای معمول برای کاهش اکسیدهای نیتروژن در گازهای خروجی، استفاده از فرآیند SCR (Selective Catalytic Reduction) با استفاده از آمونیاک به عنوان ماده اختزالی است.
مراحل اصلی این فرآیند به شرح زیر است:
تهیه آمونیاک: آمونیاک به عنوان عامل اختزال در فرآیند SCR استفاده میشود. آمونیاک میتواند به صورت مایع (محلول آبی اوره یا آمونیوم هیدروکسید) یا گازی (آمونیاک گاز) تهیه شود. در بعضی از سیستمها، آمونیاک به طور مستقیم در محل تصفیه تزریق میشود.
میکس آمونیاک با گازهای خروجی: آمونیاک با دقت و به میزان صحیحی با گازهای خروجی اکسیدهای نیتروژن مخلوط میشود.
تخلیه به کاتالیزور: مخلوط آمونیاک و گازهای خروجی به کاتالیزور واکنشی منتقل میشود. کاتالیزور معمولاً از فلزات انتقالی مانند وانادیم یا تیتانیم پلاتینه تشکیل شده است.
واکنش اختزالی (SCR): در حضور کاتالیزور، آمونیاک با اکسیدهای نیتروژن در گازهای خروجی واکنش میکند. در این واکنش، اکسیدهای نیتروژن به نیتروژن مولکولی (N2) و آب تبدیل میشوند. این واکنش باعث کاهش آلایندههای نیتروژنی موجود در گازهای خروجی میشود.
خروجی تصفیه شده: پس از عبور از کاتالیزور SCR، گازهای خروجی تصفیه شده و با غلظت کمتری از آلایندهها به محیط زیست داده میشود.
کنترل و مانیتورینگ: سیستمهای تصفیه گازهای خروجی معمولاً دارای سیستمهای کنترل و مانیتورینگ هستند که غلظت اکسیدهای نیتروژن در گازهای خروجی را کنترل میکنند تا بهینهسازی عملکرد کاتالیزور و مصرف آمونیاک انجام شود.
در کل، تصفیه گازهای خروجی با استفاده از فرآیند SCR و آمونیاک به عنوان ماده اختزالی به کاهش اکسیدهای نیتروژن در گازهای خروجی کمک میکند و در نتیجه به بهبود کیفیت هوا و کاهش آلودگی محیطی کمک میکند.
مقالات پیشنهادی:
کاتالیست هیدروژن گیری از اتیلن بنزین
منابع:
- Enriching the Earth: Fritz Haber, Carl Bosch, and the Transformation of World Food Production by Vaclav Smil (2001) ISBN 0-262-19449-X
- ↑ پرش به بالا به:۲٫۰ ۲٫۱ ۲٫۲ ۲٫۳ Hager, Thomas (2008). The Alchemy of Air. Harmony Books, New York. ISBN 978-0-307-35178-4.
- ↑ Fertilizer Industry: Processes, Pollution Control and Energy Conservation by Marshall Sittig (1979) Noyes Data Corp. , N.J. ISBN 0-8155-0734-8
- ↑ “Heterogeneous Catalysts: A study Guide”
- ↑ Smil, Vaclav (2004). Enriching the Earth: Fritz Haber, Carl Bosch, and the Transformation of World Food Production (1st ed.). Cambridge, MA: MIT. ISBN 978-0-262-69313-4.

